Una combinación de medicamentos dirigidos produce remisiones duraderas en las personas con linfoma de células B de crecimiento rápido resistente al tratamiento
- Publicación:
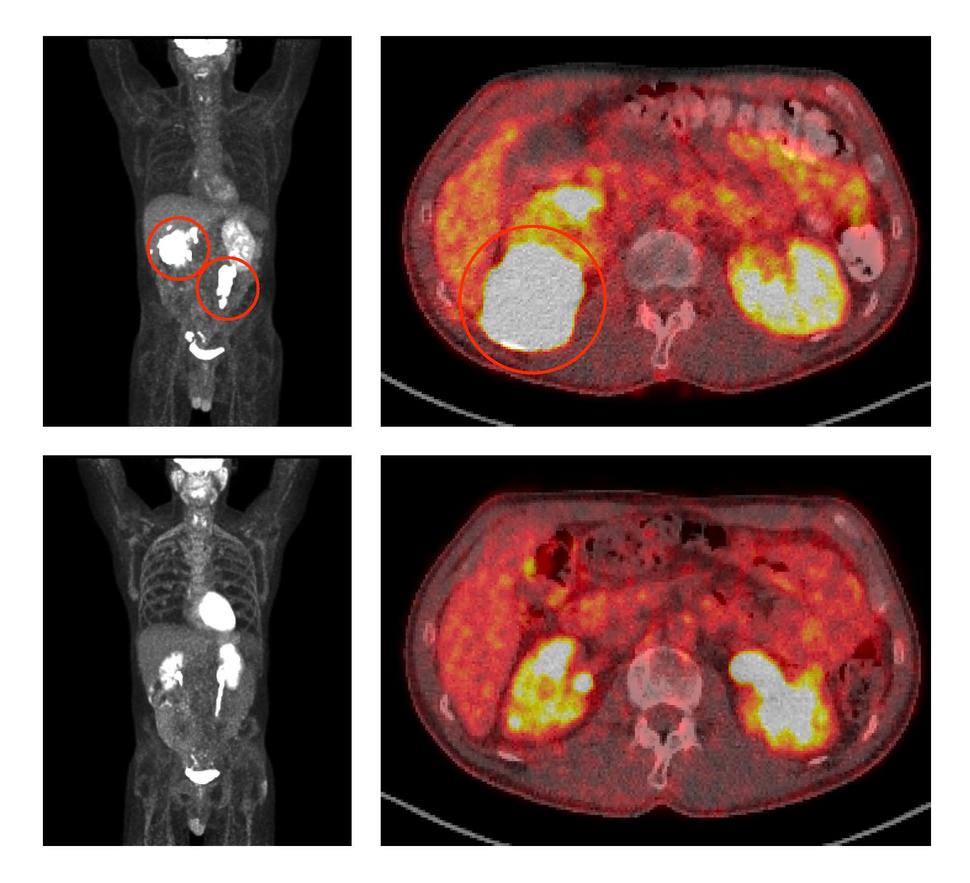
En vistas de cuerpo entero y transversales de tomografías por emisión de positrones (TEP), se observan tumores grandes de linfoma marcados con círculos antes del tratamiento con ViPOR (paneles superiores). Tras el tratamiento, los tumores desaparecieron (paneles inferiores).
Fuente: Centro de Investigación Oncológica/Instituto Nacional del Cáncer
Los investigadores de los Institutos Nacionales de la Salud (NIH) crearon un régimen de tratamiento sin quimioterapia que logra remisiones completas en algunas personas con linfoma de células B de crecimiento rápido que vuelve o ya no responde a los tratamientos estándar. La combinación de cinco medicamentos se dirige a múltiples vías moleculares que los tumores del linfoma difuso de células B grandes (LDCBG) usan para sobrevivir.
En un estudio clínico en el Instituto Nacional del Cáncer (NCI) de los NIH, los investigadores probaron la combinación de venetoclax, ibrutinib, prednisona, obinutuzumab y lenalidomida (llamada ViPOR) en 50 pacientes con LDCBG, el tipo más común de linfoma. El tratamiento achicó de forma considerable los tumores en 26 de 48 (54 %) pacientes evaluables, con la desaparición total de los tumores en 18 (38 %) de estos pacientes, lo que se conoce como una respuesta completa. A los 2 años, el 36 % de todos los pacientes estaban vivos y el 34 % no tenían la enfermedad. Estos beneficios se observaron sobre todo en las personas con dos subtipos específicos de LDCBG.
Los resultados se publicaron el 20 de junio de 2024 en la New England Journal of Medicine.
“Muchos de estos pacientes que dejaron de responder a los tratamientos estándar habrían muerto al año, y ahora una gran proporción siguen vivos después de dos años, e incluso algunos después de cuatro años”, comentó el doctor Christopher J. Melani, del Centro de Investigación Oncológica del NCI, que codirigió el estudio. “Es grato ver estas remisiones a largo plazo y las posibles curas en los pacientes”.
En los estudios anteriores, se identificaron varias vías genéticas que intervienen en el desarrollo y la supervivencia de los diferentes subtipos moleculares del LDCBG, como el similar al de célula B activada (CA) y el similar al de célula B de centro germinal (CG). Se demostró la eficacia de los medicamentos dirigidos para bloquear algunas de estas vías, pero el uso separado de los medicamentos rara vez produce respuestas duraderas en los pacientes porque los tumores quizás se vuelven resistentes al contar con otras vías de supervivencia. El doctor Melani y sus colegas plantearon la hipótesis de que la combinación de medicamentos dirigidos que bloquean vías de supervivencia múltiples llevaría a respuestas más duraderas.
Para probarla en los seres humanos, los investigadores diseñaron un régimen de cinco medicamentos a partir de estudios de laboratorio en los que analizaron qué medicamentos dirigidos tenían mayor efecto al combinarlos (sinergia) para destruir las células de LDCBG. A fin de que los medicamentos dirigidos funcionaran con sinergia en los pacientes, los investigadores administraron los medicamentos de forma simultánea en ciclos de dos semanas. Para limitar la acumulación de efectos secundarios, programaron un descanso de una semana entre cada ciclo.
“El LDCBG es uno de los cánceres con las características genéticas más heterogéneas, por eso aún no tenemos la capacidad de identificar la combinación de medicamentos exacta que sea más eficaz para un paciente determinado”, comentó el doctor Melani. “Al reunir cinco medicamentos, creemos que alguna combinación (de dos, tres o más medicamentos) en particular resultará más eficaz contra el tumor en ese paciente”.
En el estudio de fase 1b y 2, a 50 personas con LDCBG que tuvieron recaída o dejaron de responder al tratamiento se les administraron seis ciclos del régimen ViPOR. Las respuestas al ViPOR dependieron del subtipo de LDCBG. Hubo respuestas completas que se concentraron en dos subtipos, incluso en 8 de 13 (62 %) personas con LDCBG de células que no eran de CG y en 8 de 15 (53 %) personas con un LDCBG de células de CG conocido como linfoma de células B de grado alto con mutación doble.
A los 2 años, las personas con LDCBG que no era de CG y DLBCL de CG con mutación doble tuvieron tasas de supervivencia sin progresión y de supervivencia general más altas que otras personas en el estudio. El LDCBG que no es de CG y el LDCBG de CG con mutación doble dependen mucho de los mecanismos a los que se dirige ViPOR para sobrevivir, lo que explica la respuesta particularmente buena frente a la terapia combinada. El tratamiento con ViPOR también ayudó a obtener remisiones duraderas a 6 de 20 (30 %) pacientes cuyos linfomas no respondieron o volvieron tras la terapia de células T con receptor quimérico para antígenos (CAR-T), el tratamiento estándar para las personas con LDCBG recidivante.
En general, los efectos secundarios del régimen de cinco medicamentos fueron entre leves y moderados, en comparación con los de los tratamientos estándar, y se aliviaron en los períodos de descanso del tratamiento. Solo cinco pacientes tuvieron que interrumpir el tratamiento antes por motivos diferentes, incluso por los efectos secundarios. Según los investigadores, como los efectos secundarios fueron de leves a moderados, es posible que se añadan otros medicamentos a ViPOR para mejorar la eficacia del tratamiento. El equipo también estudia ahora el régimen ViPOR en las personas con otros tipos de linfoma resistentes a tratamientos anteriores.
Los investigadores iniciaron un estudio de fase 2 más grande que se realizará en varios centros para confirmar la actividad de ViPOR en las personas con LDCBG que no es de CG y LDCBG con mutación doble. Es necesario continuar la investigación para encontrar terapias para los subtipos de LDCBG de CG que no responden tan bien al régimen ViPOR.
Los investigadores del Centro de Investigación Oncológica del NCI que codirigieron el estudio con el doctor Melani fueron los doctores Wyndham H. Wilson, Mark Roschewski y Louis M. Staudt. Los investigadores del Centro Nacional para el Avance de las Ciencias Traslacionales (NCATS) de los NIH y de otras instituciones contribuyeron al estudio.
Acerca del Instituto Nacional del Cáncer: El Instituto Nacional del Cáncer (NCI) dirige el Programa Nacional del Cáncer (NCP) y las iniciativas de los Institutos Nacionales de la Salud (NIH) cuyo fin es disminuir la prevalencia del cáncer de forma drástica y mejorar la vida de las personas con cáncer. El NCI financia una variedad amplia de investigaciones y capacitaciones sobre el cáncer mediante subvenciones y contratos fuera de las instituciones. El programa de investigación intrainstitucional lleva a cabo estudios de investigación innovadora clínica y epidemiológica, transdisciplinaria básica y aplicable sobre las causas del cáncer, las formas de prevenirlo, la predicción del riesgo, la detección temprana y el tratamiento. Estos estudios incluyen las actividades de investigación en el Centro Clínico de los NIH, el hospital de investigaciones más grande del mundo. Para obtener más información en inglés sobre los estudios de investigación en el NCI, consulte el sitio web del Centro de Investigación Oncológica. Para obtener más información sobre el cáncer, visite el sitio web del NCI en cancer.gov/espanol o llame al Servicio de Información de Cáncer del NCI al 1-800-422-6237 (1-800-4-CANCER).
Acerca de los Institutos Nacionales de la Salud: Los Institutos Nacionales de la Salud (NIH) son el organismo nacional de investigación médica, integrado por 27 institutos y centros, y es un componente del Departamento de Salud y Servicios Humanos (HHS) de los Estados Unidos. Los NIH son el organismo federal principal que lleva a cabo y apoya la investigación básica, clínica y médica aplicada e investiga las causas, los tratamientos y las curas de enfermedades comunes y raras. Para obtener más información sobre los NIH y sus programas, visite salud.nih.gov.